الکتروفورز روی استات سلولز در pH قلیایی یک شیوهی ساده و مفید برای جداسازی هموگلوبینهای طبیعی و غیرطبیعی است. شناسایی کیفی و تعیین کمی انواع مختلف هموگلوبین اجازه به آشکارسازی اختلالات هموگلوبین با اهمیت بالینی را فراهم میآورد.
کاربردهای آزمایشگاهی بالینی الکتروفورز هموگلوبین
الگوی الکتروفورتیک یک فرد بالغ طبیعی، تنها انواع هموگلوبینهای فیزیولوژیکی را به نمایش میگذارد که شامل HbA1 و HbF و HbA2 میشوند و غلظت آنها در رنج نرمال قرار میگیرد (جدول ۱ را ببینید). کشف باندهای غیرطبیعی، که معمولاً در الگوهای طبیعی ظاهر نمیشوند، بیانگر حضور هموگلوبینهای غیرطبیعی در نمونهی خون است – شکل ۱ را ببینید.
| نوع هموگلوبین | ترکیب زنجیرهی گلوبین | درصد نسبت به غلطت کل هموگلوبین |
| HbA یا HbA1 | α2β2 | ۹۸ – ۹۵ ٪ |
| HbA2 | α2δ2 | ۳٬۵ – ۱٬۵ ٪ |
| HbF | α2γ2 | ۲ – ۰ ٪ |
جدول ۱ – انواع هموگلوبینهای انسانی در یک فرد بالغ طبیعی
حرکت الکتروفورتیک برخی از هموگلوبینهای غیرطبیعی بیشتر از HbA1 است و از این رو به آنها «هموگلوبینهای سریع – fast hemoglobins» گفته میشود؛ از جملهی این هموگلوبینها میتوان به HbH و HbBart’s اشاره کرد.
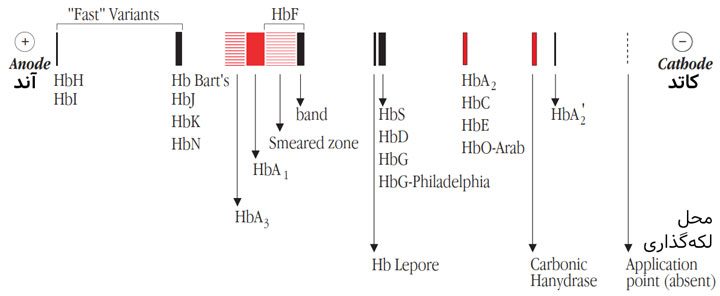
HbH: به شکل یک باند باریک (sharp) ظاهر میشود که موقعیت آن به آند نزدیکتر بوده و فاصلهاش تا HbA1 قابل مقایسه با فاصلهی HbA2 با HbA1 است.
HbBart’s: حرکتی در حد واسط HbA1 و HbH دارد؛ ظهور این نوع هموگلوبین در خون بند ناف امکان تشخیص حامل خاموش برای تالاسمی آلفا را فراهم میآورد.
روند جداسازی الکتروفورتیک هموگلوبین
آمادهسازی نمونه برای آنالیز یکی از معیارهای اصلی تاثیرگذار بر کیفیت الگوی الکتروفورتیک هموگلوبین است. محلول استفاده شده برای آنالیز، که به آن همولیزات گفته میشود، یک محلول مایع است که شامل هموگلوبینی است که توسط شکسته شدن غشای گلبولهای قرمز به وجود میآید.
مراحل پایهای آمادهسازی همولیزات عبارتاند از:
شستشوی گلبولهای قرمز: این فرایند باعث حذف باقیماندهی سرم از سطح گلبولهای قرمز میشود و که در نتیجه پروتئینهای سرم که میتوانند بر کیفیت جداسازی باندها تاثیر بگذارند، شسته میشوند.
گلبولهای قرمز از خون تام (Whole Blood) گرفته شده و با سرم فیزیولوژی (Saline – 0.9% w/v NaCl) شستشو میشوند؛ یک حجم از گلبولهای قرمز در ۹ حجم از سالین (سرم فیزیولوژی) رقیق میشود، سپس گلبولها به آرامی در محلول معلق شده و بعد سانتریفیوژ میشوند. محلول رویی را برداشته و سالین تمیز و تازه به گلبولهای قرمز اضافه شده و دوباره سانتریفیوژ میشود. مرحلهی شستشو زمانی به پایان میرسد که محلول رویی کاملاً روشن و شفاف شود.
لیز کردن گلبولهای قرمز: این مرحله برای استخراج هموگلوبین از گلبولهای قرمز است. لیز کردن توسط شوک اسمزی به گلبولهای قرمز انجام میشود، برای مثال از آب مقطر استفاده میشود.
در واقع آب مقطر به گلبولهای قرمزِ شستهشده اضافه میشود. غلظت نهایی هموگلوبین در همولیزات باید بین ۳ تا ۴ گرم بر دسیلیتر (g/dl) باشد، از این رو حجم آب مقطر اضافهشده تابعی از غلظت هموگلوبین در نمونهی خون است. برای مثال، اگر غلظت هموگلوبین کل در خون تام برابر ۱۲ گرم بر دسیلیتر (g/dl) باشد، ۱ میلیلیتر از گلبول قرمز شستهشده، با آب مقطر به حجم ۴ میلیلیتر رسانده میشود. بعد از مرحلهی لیز کردن، محلول سانتریفیوژ شده تا باقیماندههای سلول (cell debris) حذف شوند.
نمونهبرداری از همولیزات: این مهمترین مرحلهی فرآیند است؛ نمونهبرداری صحیح در محلول حاوی هموگلوبین از آلودگی توسط باقیماندههای سلول (cell debris) پیشگیری میکند، که بر کیفیت جداسازی (migration) و در نهایت بر کیفیت الگوی الکتروفورتیک تاثیر میگذارد.
بعد از مرحلهی سانتریفیوژ کردن، محلول درون لولهی آزمایش در قسمت بالا به صورت قرمز و شفاف و در انتهای لوله معمولاً متراکم، کدر و ژلمانند ظاهر میشود. همولیزات باید از ناحیهی شفاف نمونهبرداری شود؛ به عبارتی باید از قسمت بالایی محلول. استفاده از محلول متراکم و کدر یک الگوی الکتروفورتیک لکهدار (smeared) ایجاد نموده که تشخیص باندها را دشوار میکند. گاهی اوقات محلول همولیزات به صورت یک دست شفاف و قرمز ظاهر میشود، به عبارتی دیگر هیچ تفاوت ظاهریای مشاهده نمیشود. در این مواقع نیز همولیزات باید همیشه از قسمت بالایی محلول نمونهبردای شود.
نمونهی همولیزات بهتر است در کمتر از یک ساعت پس از آمادهسازی استفاده شود. از آنجا که محلول همولیزات تنها برای زمان کوتاهی پایدار است، توصیه میشود که نمونه خون تام نگهداری شده و همولیزات در همان روز انجام آزمایش الکتروفورز، تهیه شود. جداسازی الکتروفورتیک (Electrophoretic separation) همولیزات، که در pH قلیایی با محلول بافری با یک قدرت یونی پایین انجام میشود، پروتئینهای درون گلبولهای قرمز، از جمله هموگلوبینها و یک آنزیم به نام کربنیک انهیدراز، جدا خواهند شد.
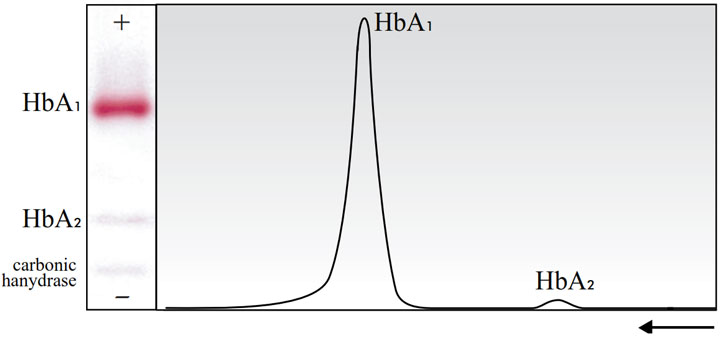
یک الگوی الکتروفورتیک از یک همولیزات طبیعی، باندهای HbA1 (نزدیکترین به آند)، HbA2 و کربنیک انهیدراز (نزدیکترین به کاتد) را نمایش خواهد داد.
کاغذ باید به صورت کامل رنگبری شود تا پسزمینهای شفاف ایجاد کند که امکان کشف باندها را سادهتر سازد. باقیماندهی ملایمی از رنگ روی پسزمینه ممکن است از تشخیص صحیح باند HbA2، که معمولاً غلظت پایینی (۲ تا ۳ درصد) دارد، یا HbF، که حتی تا ۷-۸ درصد از هموگلوبین کل هم باند واضحی تشکیل نمیدهد و تنها یک باند کشیده شده (smeared band) در سمت کاتدی HbA1 ایجاد میکند، جلوگیری کند.
خصوصیات الگوی الکتروفورتیک هموگلوبین
در ادامه لیستی از برخی مشخصههای کیفی الگوی یک هموگلوبین طبیعی آمده است.
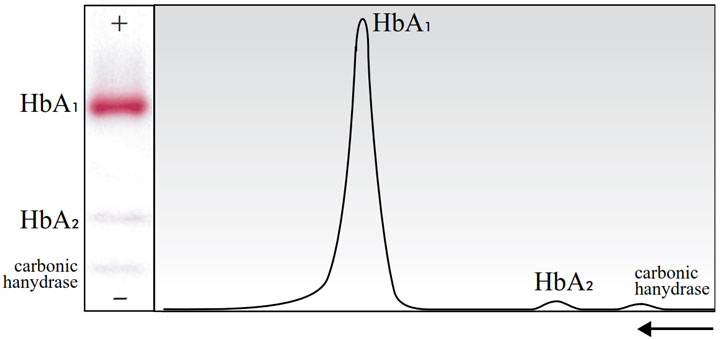
- باند HbA1 فراوانترین نوع هموگلوبین در گلبول قرمز است، از این رو شایعترین باند در الگو بوده و به سادگی قابل تشخیص است؛ این باند یک شکل معینی شبیه آلبومین در الگوی الکتروفورتیک پروتئین سرم دارد، و دارای ظاهری یکنواخت در سمت کاتدی و یک کشیدگی ملایم (mild smearing) در سمت آندی است.
- باند HbA2 معمولاً باندی کوچک و متمرکز است، گرچه به صورت ملایمی رنگ میگیرد.
- باندهای HbA1 و HbA2 به خوبی جدا شده و از هم فاصله میگیرند و فضای بین آنها بیرنگ خواهد بود.
- باند کربنیک انهیدراز کوچک بوده و به خوبی متمرکز است؛ که حتی در شرایطی بالینی که غلظت باندهای هموگلوبین غیرطبیعی زیادی نشان داده میشود با شدت ثابتی رنگ میگیرد.
- باندهای HbA2 و کربنیک انهیدراز به خوبی جدا شده و از هم فاصله میگیرند. متمرکز بودن و جدا شدن این دو باند مهمترین نشانههای کیفیت الگوی الکتروفورتیک هموگلوبینها هستند.
تفسیر نتایج الکتروفورز هموگلوبین
زمانیکه باندها تحرک الکتروفورتیک متفاوتی داشته باشند، تشخیص انواع مختلف هموگلوبین امکانپذیر است. از آنجا که هویت باندهای جداشده با توجه به مکان قرارگیری آنها در الگو، به آنها اختصاص داده میشود، الگوی نمونه با محلول هموگلوبین مرجع (نمونهی کنترل) همواره باید مقایسه شود. این محلول معمولاً شامل مخلوطی متعادل از Hbs, HbF, HbA1 و HbA2 است و امکان مقایسهی مکان هر دو نوع باندهای طبیعی و غیرطبیعی با الگوی هموگلوبین مرجع (نمونهی کنترل) را فراهم میکند. (شکل ۳ را ببینید.).
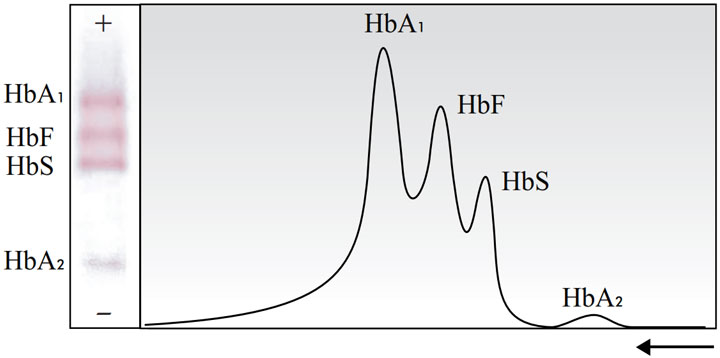
نمودار بهدست آمده از دانسیتومتری الگوی هموگلوبین برای ارزیابی کیفی، نباید هیچوقت شامل کربنیک انهیدراز باشد (شکل ۴ را ببینید.).
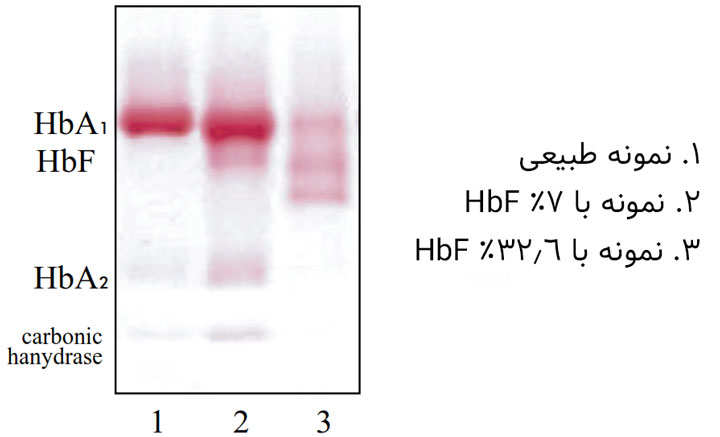
هموگلوبین F (همان HbF) در غلظتهای پایینتر از ۷-۸ درصد از هموگلوبین کل، یک باند واضح (sharp) ایجاد نمیکند، بلکه یک باند کشیده شده (smeared) که خیلی کم رنگ میگیرد را در سمت کاتدی HbA1 تشکیل میدهد.
تمرکز باند HbF با افزایش غلظت، بهبود پیدا میکند؛ از این رو، وقتی غلظت به ۱۰-۱۵ درصد برسد، یک باند واضح (sharp) در الگو مشاهده میشود، اگرچه باندهای HbA1 و HbF توسط یک ناحیهی کشیدهشده (smeared zone) به هم متصل میشوند که رنگ زیادی رو به خود میگیرد (شکل ۵ را ببینید.).
جدول ذیل، هموگلوبینهای طبیعی و غیرطبیعی را که در الگوی الکتروفورتیک براساس تحرک و/یا غلظت (که به صورت درصدی از هموگلوبین کل بیان میشود) قابل شناسایی هستند، لیست شده است.
| نوع Hb | غلظت | نکات |
| HbH
HbI |
۵ تا ۱۵ درصد
در موارد نادر ۳۰ تا ۴۰ درصد
حدود ۲۵ درصد |
باند «سریع»؛ هر دو تحرک مشابهی نشان میدهند و به یک اندازه از HbA1 فاصله میگیرند؛ برابر با فاصلهی HbA1 و HbA2 |
| Hb Bart’s | باند «سریع»؛ تحرک آن در حد فاصل HbA1 و HbH است | |
| HbJ | کمی کاتدیکتر نسبت به Hb Bart’s | |
| HbA3 | ترکیبی از هموگلوبینهای گلیکوزیله است و شبیه یک ناحیهی کشیدهشدهای که کمی رنگ گرفته، قبل از HbA1 ظاهر میشود. | |
| HbA1 | ۹۵ تا ۹۸ درصد | |
| HbF | کمتر از ۲ درصد | زمانی که غلظت آن پایین باشد، قابل تشخیص از HbA1 نیست. |
| Hb Lepore | ۱۰ تا ۱۵ درصد | کمی آندیکتر از HbS |
| HbS | ۲۵ تا ۴۵ درصد | فارغ از غلظتش، یک باند واضح و پررنگ ایجاد میکند و در حد فاصل HbA1 و HbA2 متمرکز میشود. |
| HbA2 | ۱.۵ تا ۳.۵ درصد | مقادیری بین ۳.۶ تا ۹ درصد نشانهی سندرومهای تالاسمی هستند. HbA2 به ندرت بیشتر از ۱۰ درصد میشود. مقادیر بالاتر احتمالاً ناشی از حضور HbC و HbO-Arab و HbE باشد که به اندازهی HbA2 تحرک دارند و در محل مشابه متمرکز میشوند. |
| HbA’2 | ۱.۵ تا ۳.۵ درصد | گونهی غیر پاتولوژیک HbA2 |
جدول ۲ – انواع هموگلوبینهای طبیعی و غیرطبیعی انسانی در الگوی الکتروفورتیک با توجه به تحرک و غلظت
هنگام تفسیر الگوهای هموگلوبین، بسیار مهم است بدانیم که تعداد زیادی از باندهای غیرطبیعی، تحرکهای الکتروفورتیک مشابه یا برابری را به نمایش میگذارند که تشخیص انواع مختلف هموگلوبین را دشوار میکنند (شکل ۶ را ببینید.).
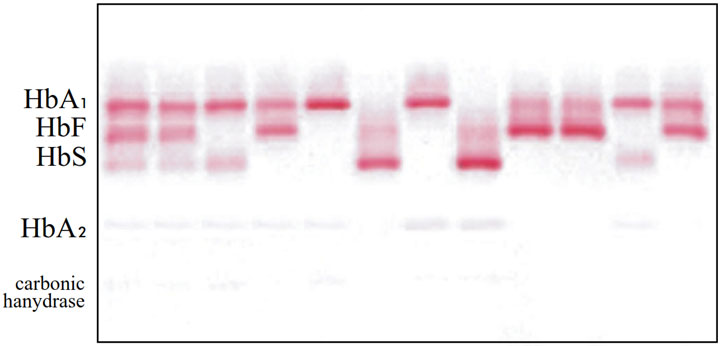
انجام آزمایشهای دیگر با سایر روشهای الکتروفورز، امکان برطرف کردن موارد دشوار تشخیص هموگلوبینهای غیرطبیعی را ممکن میسازد.

دیدگاه بگذارید